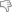-
Michiko5389.
User deleted
Sul resto non mi esprimo, perché dopo due anni e mezzo credo di non ricordare più niente! XD
Poi ce l'avevano spiegata malissimo... -.-. -
Elisa".
User deleted
Ok, so che è festa..ma per me non esistono festività ora 
1 Guardate qui:
Nella reazione c'è una specie (l'ho contrassegnata con un asterisco). Ecco, lì ci sono 2 ossigeni che sono possibili nucleofili..perchè reagisce l'ossigeno carbonilico e non quello del gruppo OH? E' più nucleofilo? Ma quale è la ragione?
2 Poi..mi sapreste dire perchè il 4-metossifenolo è più acido del 4-clorofenolo considerando le loro basi coniugate?
Grazieee. -
~Elettrone.
User deleted
1) In realtà è indifferente quale dei due ossigeni fai reagire, il prodotto che ottieni è sempre lo stesso. Te ne rendi facilmente conto se pensi che in ambiente acido anche il carbossile è protonato. Per l'acido carbossilico protonato puoi scrivere due strutture di risonanza equivalenti in cui la carica positiva sta una volta su di un ossigeno e una volta sull'altra (in altre parole, tutti e due gli ossigeni hanno la stessa densità di carica e quindi anche la stessa reattività). SPOILER (clicca per visualizzare)
2) C'è un errore: il 4-clorofenolo è più acido del 4-metossifenolo (sulle slides del mio prof porta che i pka sono di 9.2 per il 4-clorofenolo e 10.2 per il 4-metossifenolo). La base coniugata è stabilizzata da gruppi elettron-attrattori in orto e para all'OH, che sono le posizioni dove viene delocalizzata la carica negativa sull'anello.
Sia il metossile che il cloro sono attrattori per effetto induttivo e donatori per effetto mesomerico, ma:
il CH3 (elettron-repulsore) rende l'ossigeno più denso di carica negativa e quindi più propenso a donare che ad attrarre elettroni;
il Cl è un donatore peggiore dell'ossigeno perché i suoi doppietti stanno in orbitali 3p (quelli dell'ossigeno nei 2p), quindi la sovrapposizione con i 2p del carbonio è più scarsa.
In sostanza il cloro stabilizza meglio la carica negativa quindi rende il fenolo più acido. .
. -
Elisa".
User deleted
mmm il mio prof ha scritto nel testo dell'ese che il metossifenolo ha pKa=10^-10 e il clorofenolo ha pKa=10^8
Quindi ha detto lui una cavolata? Perchè se non ricordo male io..a pka minore aumenta l'acidità. No?. -
~Elettrone.
User deleted
Eli quelli che hai scritto tu sono le Ka, non i pKa 
Sì, l'acidità aumenta al diminuire del pKa, perché pKa= -logKa, quindi la specie col pKa più piccolo ha la costante di dissociazione acida più alta.
Ka=10^-10 => pKa=10
Ka=10^-8 => pKa=8
Il clorofenolo è più acido .
. -
Elisa".
User deleted
Ma sull'esercizio c'erano le pka.. o.0
in ogni caso..non vi romperò più perchè.....l'esame l'ho passato! .
. -
~Elettrone.
User deleted
Mha... ha sbagliato il testo allora!
Grandeeeeee! Io ne avrò ancora per molto invece... ç_ç. -
Elisa".
User deleted
 Beh Linda..diciamo che tu la chimica te la sei sposata! xD
.
Beh Linda..diciamo che tu la chimica te la sei sposata! xD
. -
~Elettrone.
User deleted
Ma sì ♥
solo che l'organica è di una noiaaa... sempre gli stessi concetti: risonanza, chi è più acido, chi è più nucleofilo, chi reagisce prima, reazioni che portano a stessi prodotti con stereochimiche diverse se usi questo reagente o quell'altro... aaaaaaaaaaaaaaaaaaaaaaaa
ok era più un post da "sfoghi" ma lasciatemelo passare dopo una giornata passata a studiare organica avanzata ç_ç. -
Elisa".
User deleted
Non è la prima volta che sento qualcuno dire che la chimica organica è sempre quella, che è noiosa..e ogni volta rimango sconcertata quando sento queste cose muahuahauhau .
Maledetta organica.. |